Por vezes sentimos que aquilo que fazemos não é senão uma gota de água no mar. Mas o mar seria menor se lhe faltasse uma gota.
Madre Teresa de Calcutá
Como funcionam moléculas de água? Quais as características da água? Bem, essas são dúvidas de muitos de nossos leitores!
A água, com sua fórmula química H₂O, é uma substância com várias funções em nosso planeta, desde sustentar a vida até regular o clima. Cada molécula de água consiste em dois átomos de hidrogênio covalentemente ligados a um átomo de oxigênio, formando um ângulo que confere à molécula uma natureza polar.

Esta polaridade é responsável por muitas das propriedades extraordinárias da água, incluindo sua habilidade em dissolver muitos tipos de substâncias, seu alto calor específico, sua expansão ao congelar e sua capacidade de atuar como solvente universal.
Aliás, entre os cientistas que contribuíram para nosso entendimento das propriedades da água está Henry Cavendish, que no século XVIII identificou a água como um composto de hidrogênio e oxigênio.
Johannes van der Waals e Gilbert Lewis, posteriormente, ajudaram a elucidar a natureza da ligação e das forças intermoleculares que explicam o comportamento único da água.
Livros que abordam a química e as propriedades da água incluem "Water: A Comprehensive Treatise" de Felix Franks, que oferece uma análise de seus aspectos físico-químicos, e "The Science of Water: Concepts and Applications" de Frank R. Spellman, que discute a importância da água nas ciências ambientais e em aplicações práticas.
Em no artigo de hoje, falarei mais sobre a composição das moléculas da água na química. Vem comigo!

Composição química da água
A água é uma substância química composta por dois elementos: hidrogênio e oxigênio, na proporção de dois para um, resultando na fórmula molecular H₂O.
Cada molécula de água consiste em um átomo de oxigênio ligado a dois átomos de hidrogênio por ligações covalentes, formando um ângulo de aproximadamente 104.5° entre os átomos de hidrogênio. Essa estrutura angular confere à água muitas de suas propriedades, como sua capacidade de solvatar uma variedade de substâncias e sua expansão ao congelar.
Quer reforçar conceitos? Faça uma aula de quimica 1 ano do ensino medio.
Quem descobriu a composição química da água?
A descoberta da composição química da água é atribuída a Henry Cavendish, um químico e físico britânico, no final do século XVIII. No entanto, embora o papel de Cavendish tenha sido muito importante, a compreensão completa da composição da água foi o resultado de um esforço colaborativo envolvendo vários cientistas ao longo do tempo.
Henry Cavendish realizou experimentos que envolviam a passagem de correntes elétricas através da água, um processo conhecido como eletrólise, resultando na liberação de gases hidrogênio e oxigênio.
Cavendish não apenas isolou o hidrogênio, que ele chamou de "ar inflamável", mas também sugeriu que a água era uma substância composta, formada pela combinação de hidrogênio com um componente de ar que ele não identificou como oxigênio.
Mais tarde, Antoine Lavoisier, junto com outros cientistas, construiu sobre as descobertas de Cavendish, realizando combustão de hidrogênio no ar e produzindo água, assim identificando e nomeando o oxigênio e concluindo definitivamente que a água era uma molécula composta por hidrogênio e oxigênio.
Polaridade e coesão
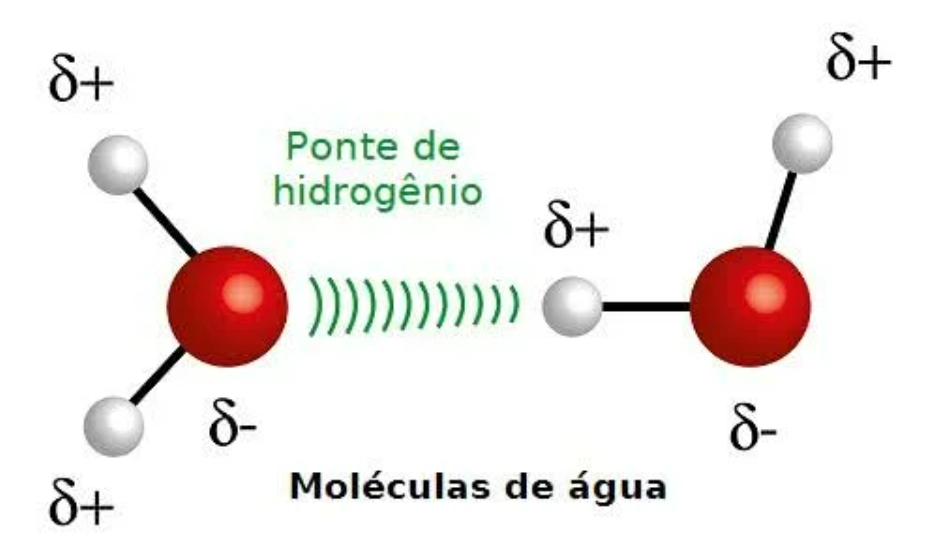
A água é uma molécula polar, o que significa que tem uma extremidade ligeiramente negativa (o oxigênio) e extremidades ligeiramente positivas (os hidrogênios). Essa polaridade permite que as moléculas de água formem ligações de hidrogênio entre si, resultando em altos pontos de ebulição e fusão para uma molécula de seu tamanho e conferindo propriedades como coesão e adesão.
Solvente universal
Devido à sua polaridade e capacidade de formar ligações de hidrogênio, a água é capaz de dissolver muitos tipos de substâncias, tornando-se o solvente universal. Esse é um fator que permite a vida na Terra, facilitando reações químicas dentro de organismos vivos e transportando substâncias.
Densidade anômala
A água tem a propriedade incomum de expandir-se quando congela. A maioria das substâncias se torna mais densa na forma sólida, mas a água atinge sua máxima densidade a 4°C.
Quando se congela a 0°C, sua estrutura cristalina mantém as moléculas mais afastadas do que no estado líquido, tornando o gelo menos denso que a água líquida. Essa propriedade tem implicações ecológicas significativas, permitindo que a vida aquática sobreviva sob a superfície congelada de corpos de água durante o inverno.
Capacidade térmica
A água tem uma alta capacidade térmica. Logo, é possível absorver ou liberar grandes quantidades de calor com pouca mudança em sua própria temperatura. Assim, ajuda a regular o clima da Terra, proporcionando um ambiente estável para o desenvolvimento da vida.
Quais as principais propriedades químicas da água?
A água ostenta uma série de propriedades químicas que a tornam necessária para a vida na Terra, influenciando muitos processos naturais e humanos. Essas propriedades derivam da estrutura molecular da água e das interações entre suas moléculas.
Cada molécula de água tem uma distribuição desigual de carga elétrica, tornando-a polar. Assim, significa que a molécula tem um lado positivo, onde os átomos de hidrogênio estão, e um lado negativo, no átomo de oxigênio. A polaridade permite que a água forme ligações de hidrogênio fortes com outras moléculas de água e com outras substâncias polares.
Devido à sua polaridade e capacidade de formar ligações de hidrogênio, a água é capaz de dissolver mais substâncias do que qualquer outro líquido. Além disso, a água tem uma das mais altas capacidades térmicas entre as substâncias comuns. Pode absorver ou liberar grandes quantidades de calor sem sofrer uma grande mudança de temperatura. Essa propriedade ajuda a regular o clima da Terra e permite que os organismos vivos mantenham a homeostase térmica.
Ao contrário da maioria das substâncias, a água expande-se e torna-se menos densa quando congela. Isso ocorre porque as ligações de hidrogênio estabilizam a estrutura molecular do gelo em uma forma cristalina aberta. Como resultado, o gelo flutua na água líquida.
Tensão superficial elevada
A água tem uma tensão superficial relativamente alta devido às ligações de hidrogênio entre as moléculas de água, possibilitando que forme gotas e que insetos, como o arrepiante-d'água, caminhem sobre sua superfície.

Essa propriedade também serve para processos como a capilaridade, que ajuda as plantas a transportar água de suas raízes para as folhas.
Produto iônico da água (Kw)
A autoionização da água, onde uma molécula de água doa um próton (H⁺) para outra, formando íons hidrônio (H₃O⁺) e hidróxido (OH⁻), define o produto iônico da água (Kw). Esse equilíbrio entre a formação de íons hidrônio e hidróxido determina o pH de soluções aquosas.
O que é a qualidade da água?
A qualidade da água refere-se às características físicas, químicas e biológicas da água, que determinam sua adequação para uma variedade de usos, seja para consumo humano, atividades agrícolas, industriais, recreativas ou ambientais.
Avaliar a qualidade da água envolve medir a presença e as concentrações de diversos contaminantes, assim como avaliar propriedades como a temperatura, o pH, a turbidez e a presença de nutrientes e microorganismos.
Uma boa qualidade de água implica que ela está livre de poluentes prejudiciais em níveis que possam afetar a saúde humana ou o ambiente, e contém minerais e outros constituintes em quantidades que atendam aos padrões e diretrizes estabelecidos por autoridades sanitárias e ambientais.
A importância da qualidade da água é enorme, impactando a saúde humana, os ecossistemas aquáticos e terrestres, a biodiversidade, a agricultura, a pesca, a indústria e o turismo.
A degradação da qualidade da água, como consequência, leva a problemas de saúde pública, como surtos de doenças transmitidas pela água, perda de habitat para a vida selvagem, redução da produtividade agrícola devido à salinização ou contaminação por nitratos, e restrições ao uso industrial da água devido à presença de substâncias tóxicas.
Como medimos a qualidade da água?
A medição da qualidade da água é um processo complexo que envolve a coleta e análise de amostras de água, utilizando uma variedade de métodos e tecnologias.
Essas medições são realizadas in situ (no local) ou em laboratório, e abrangem muitos tipos de parâmetros físicos, químicos e biológicos.
Alguns dos principais métodos e parâmetros utilizados para avaliar a qualidade da água incluem:
Parâmetros físicos
Incluem temperatura, turbidez (clareza da água) e cor. Esses parâmetros são importantes porque influenciam a vida aquática e a usabilidade da água para consumo humano e outros fins.
Parâmetros químicos
Incluem o pH, a condutividade elétrica (que indica a presença de íons solúveis), o oxigênio dissolvido (OD), a demanda bioquímica de oxigênio (DBO), a demanda química de oxigênio (DQO), nitratos, fosfatos, metais pesados e contaminantes orgânicos persistentes (COPs).
Esses parâmetros ajudam a avaliar a presença de substâncias potencialmente tóxicas e a capacidade da água de sustentar a vida aquática.
Parâmetros biológicos
Envolvem a identificação e quantificação de bactérias patogênicas, vírus, algas e outros microorganismos. O teste mais comum é a contagem de coliformes fecais, que serve como indicador de contaminação fecal e, consequentemente, da presença de agentes patogênicos.
Monitoramento e avaliação ecológica
Além de testes diretos de parâmetros físicos, químicos e biológicos, a avaliação da qualidade da água também inclui o monitoramento da biodiversidade aquática, incluindo a presença e a saúde de espécies específicas de plantas e animais, que podem servir como indicadores da saúde geral do ecossistema aquático.
Conforme deve imaginar, é válido salientar que a avaliação da qualidade da água assegura que os recursos hídricos atendam às necessidades de todos os usuários, protegendo a saúde humana e preservando o meio ambiente.
E então, tem mais alguma dúvida ou curiosidade sobre moléculas da água que não citamos no conteúdo?
Resumir com IA:
















